中国有11款新冠疫苗进入临床试验(后悔参加临床试验)
1. 中国新冠疫苗研发进展:11款疫苗进入临床试验阶段
1.1 中国新冠疫苗研发的全球领先地位
中国在新冠疫苗研发领域走在世界前列,已经成为全球抗疫的重要力量。目前已有11款新冠疫苗进入临床试验阶段,覆盖了多种技术路线,展现了强大的科研实力和组织能力。这种领先地位不仅体现在数量上,更体现在质量与效率上。国家在短时间内完成了从实验室研究到临床试验的跨越,为全球疫情防控提供了有力支持。
1.2 11款疫苗的技术路线与临床阶段分布
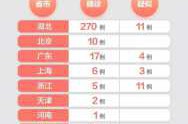
这11款疫苗分别采用了不同的技术路线,包括灭活疫苗、腺病毒载体疫苗、重组蛋白疫苗、核酸疫苗以及减毒流感病毒载体疫苗等。其中,4款疫苗已经进入Ⅲ期临床试验,包括3款灭活疫苗和1款腺病毒载体疫苗。其余疫苗则在Ⅰ期或Ⅱ期试验中稳步推进。这样的布局不仅体现了技术多样性,也为后续大规模接种提供了更多选择。
1.3 国家药监局对疫苗安全性和有效性的严格把控
国家药监局在新冠疫苗研发过程中发挥了关键作用,确保每一款疫苗都符合严格的审批标准。疫苗用于健康人群,其安全性与有效性必须经过科学验证。国家药监局通过多轮审查、数据比对和专家评估,保障了疫苗的质量。同时,国内企业也加快了生产线建设,确保疫苗能够稳定供应,满足国内外需求。
2. 新冠疫苗临床试验中的副作用与风险分析
2.1 常见的新冠疫苗副作用及其应对措施
新冠疫苗在研发过程中,会经历多轮试验,以确保其安全性。在临床试验中,参与者可能会出现一些常见的副作用,比如注射部位红肿、发热、乏力、头痛等。这些反应通常是轻微且短暂的,多数情况下会在几天内自行消失。对于这些常见症状,研究人员会提前告知受试者,并提供相应的应对建议,如休息、多喝水或服用退烧药等。
2.2 参加新冠疫苗临床试验的风险和注意事项
参与新冠疫苗临床试验意味着要承担一定的风险,虽然这些风险通常被严格控制,但仍然需要参与者充分了解。例如,某些疫苗可能在个别案例中引发更严重的不良反应,尽管概率极低。因此,在参加试验前,受试者需要接受详细的健康评估,并签署知情同意书。同时,试验期间需定期进行体检和数据记录,确保一旦出现异常情况能够及时处理。
2.3 疫苗安全性数据的公开与公众信任建立
为了增强公众对疫苗的信心,国家和企业会逐步公开疫苗的安全性数据。这些数据包括临床试验中观察到的所有副作用、发生频率以及处理方式。通过透明的信息披露,公众可以更好地理解疫苗的潜在风险与收益。此外,权威机构也会发布相关报告,帮助媒体和公众正确解读数据,避免误解和恐慌情绪的蔓延。
3. 从“后悔参加临床试验”看公众参与意愿与信息透明度
3.1 公众对新冠疫苗临床试验的认知与误解
在新冠疫苗研发过程中,公众对临床试验的了解程度参差不齐。有些人可能因为网络上的不实信息或片面报道,对临床试验产生恐惧心理。比如,有人误以为所有参与试验的人都会面临严重健康风险,或者认为试验结果不透明、缺乏科学依据。这种认知偏差会让一部分人对参与试验持保留态度,甚至出现“后悔参加”的情绪。
3.2 临床试验参与者的真实体验与反馈
实际参与新冠疫苗临床试验的人群中,大多数反馈是积极的。他们表示,在试验过程中得到了充分的医疗支持和信息告知,整个流程规范且有条不紊。然而,也有一部分人因信息沟通不畅或预期与现实不符而感到失望。例如,某些参与者可能对试验目的理解不清,或是对后续跟踪观察的要求感到困扰。这些真实体验反映出信息传递的重要性,以及公众对试验过程透明度的期待。
3.3 提高信息透明度,增强公众参与信心
要提升公众对临床试验的信任度,关键在于提高信息透明度。一方面,科研机构和企业需要主动公开试验进展、数据变化和潜在风险,避免信息孤岛现象。另一方面,媒体和科普平台也应承担起责任,用通俗易懂的语言向大众解释临床试验的意义和流程。只有当公众真正了解试验的价值和安全性,才能更愿意参与到这一关乎全人类健康的伟大事业中。
本文系作者个人观点,不代表必修号立场,转载请注明出处!